表1 体幹部定位放射線治療計画手順
|
||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||
上半身の皮膚を充分露出し,全例にvacuum pillowを作成している。長時間同一姿勢を安楽に保つことに役立っている。 |
||
両手挙上が必要な場合,arm supportを使用。 |
||
アイソセンター,その頭尾側の体表皮膚,両腕など最低8〜11カ所に皮膚マーキング。 |
||
原則として呼吸抑制用の腹壁圧迫は行っていない。呼吸同期装置が使用不可だった一例で腹帯を使用し横隔膜の動きを1cm以下になることを透視下で確認し治療した。 |
ただ「箱」の中に身体が入っているだけである。 |
||
照射中に患者が動くと再セットアップが必要になる。治療時間がさらに長くなり,患者の苦痛増加や照射精度低下などの懸念がある。 |
呼吸(腹壁の動き)を感知するセンサーが2種類あり,事前確認し感度の高い方を採用している。 |
||
呼吸同期照射法の最大の利点は,照射容積を50% 前後減少できる点である。当院では諸家の報告を踏まえ,安静呼気相30% 領域で照射することを原則としている。 |
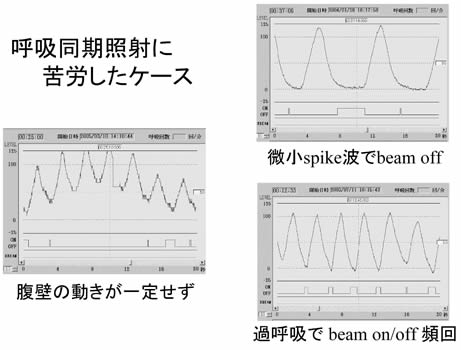
実際の呼吸曲線が予測波型とずれたり,spike波が出ると照射停止してしまう(図2)。 |
||
呼吸波形が一旦ずれると修正する手間がかかる。呼吸同期無しの時より照射時間が数倍かかる。 |
||
呼吸同期装置を放射線治療室から移動できないため,X線シミュレータ下での病巣の動きと呼吸波形とのずれの検証が不可能。 |
呼吸感知センサーがガントリーと物理的に干渉する(図3)。 |
||
呼吸同期照射の有無で,局所制御,合併症の程度及び頻度に差がでるのか明確でない。 |
||
2005年6月時点で放射線治療への呼吸同期装置使用が薬事未承認である。ちなみに,当院を含め既納入装置に関しては行政への届け出により使用可能となっている。 |
CT撮像前に仮の体表マーキングを行い,撮像後に改めて位置のずれがないか再確認している。 |
||
Gross tumor volumeが上肺野や背側の場合,両腕挙上させている。 |
||
CTは5 mm厚,5 mm幅スライスで,Gross tumor volume中心に頭尾側30〜50 cm程度を範囲。肺は全肺野,肝は全肝撮像を原則。 |
||
安静時呼気,自発呼吸停止下で撮像している。 |
ライナックと治療計画CTの寝台が別であり,撮像後に一旦固定具から身体が離れる必要がある。照射位置再現性の点で不安。 |
||
前もって安静呼気位での呼吸停止の練習は充分行うが,実際に撮像したCT像が正確な安静呼気相かどうかわからず,患者を信じるしかない。2005年4月にCTを呼吸同期対応にバージョンアップした(未使用未検証)。 |
||
CT寝台自体のたわみ,ずれ。当院では診断CT兼用で薄い平板をただ載せているだけ。治療計画専用寝台を用いるべきなのだが。 |
照射直前に毎回正側2方向ライナックグラフィー(LG)を撮像。腫瘍自体あるいは事前に挿入した体内金マーカーのX線シミュレーター写真,または放射線治療計画装置で作成した再構成画像(DRR)と照合し,X,Y, Z座標3方向でずれが5 mm以内の誤差になる事を視認 位置修正している。 |
||
金マーカーは肝では原則挿入。挿入部が腫瘍内だとアーチファクトでCT上GTV描出困難となるので,腫瘍から数cm離れた肝内に超音波ガイド下で留置。肺では3例のみに施行した。 |
肺の症例は肺気腫,肺機能低下例が多く,経皮的金マーカー挿入は気胸の恐れがある。但し,留置しないと腫瘍確認や位置照合が困難な事がある。 |
||
LGでの金マーカー同定率が高くない。肝ではマーカー留置11例(照射回数36回)中,視認不能が正面 14回(39%),側面16回(44%)もあった。肺ではマーカー留置3例(照射回数9回)のうちマーカー視認不能は0回であった。 |
||
金マーカーも腫瘍自体もLGで確認できない場合は,周囲組織の解剖学的照合で間接的に確認し「エイヤッ !」と照射するしかない。 |
||
治療中の位置確認は,LG撮像後は時間的制約もあり皮膚面での確認しか行っていない。 |
3次元放射線治療計画装置を用いて,non-coplanar固定7-9門の3次元原体照射を計画,原則としてPlanning
target volume中心に総線量45 Gy/3回/3日間を処方している。 |
||
X線エネルギーは,肺では4 MV,肝では10 MVを用いている。線量計算は肺などの不均質補正ありとしている。 |
||
治療計画に1日,実際の照射は翌日以降に連続3日間を原則としている。 |