2) 当センターにおける体幹部定位放射線治療の現状
有 賀 久 哲・久保園 正 樹
角 藤 芳 久
宮城県立がんセンターでは,2004年度の機器更新を機会に体幹部に対する定位放射線治療の導入を決定し,同年12月より治療を開始,これまでに3患者に対し実施している。システム導入にあたっては想定外の問題点 装置の不備等のトラブルも多少経験したが,まずは治療患者の適応を絞ること,透視画像を基準とした確認手順を見直すことで,精度を確保した治療が実施できていると考える。今後は,治療成績に基づきながら,適応拡大 設備拡充を図っていきたい。
当センターは,ベッド数383床のがん専門病院で,年間新患数550例程の放射線治療を行っている。頭頸部腫瘍に対する定位放射線治療は1994年より開始して240例を越える実績があるが,体幹部の定位照射についてはこれまで経験がなかった。
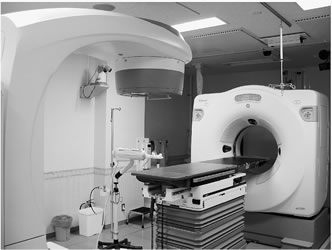
Fig. 1
|
2004年4月の健保収載と当院の機器更新が重なったため,体幹部の定位放射線治療を考慮した施設整備を行うことができ,まさに新治療の導入を行ったところである。主な新規更新装置は,呼吸同期を標準装備するClinac 21EX (バリアン社),治療計画CTとX線シミュレータとを共通寝台でつなぐSmart Gantry System(バリアン社,Fig. 1),患者固定装置VAC-LOK(東洋メディック),治療計画装置XiO(CMS)等である。On-board imagerのようなImage Guided Radiotherapyを実現するオプションも無くはなかったが,予算的に全く実現不能であった。
施設として定位型手術枠を用いる高精度照射に関する蓄積があったため,メカニカルな意味での精度保証は継続的に対応できており,問題はinternal motionを伴う体幹部病変への照準精度をいかに保証するかであった。治療時にターゲットの位置をモニタすることが本質的な解決策として必要と思われるが,そのような装置がまだ普及しているとはいえない現在,何らかの “工夫”が必要となる。検討の末,位置的不確実性を補うためには「マージンをしっかり取る」しかないと結論し,基本方針とした。当施設で腫瘍の動きを直接把握できるモダリティはX線シミュレータのみであるため,照射野設定の基本画像はX線透視像と決め,透視上でinternal target volume (ITV) を確認できない腫瘍は適応外とすることにした。息止め等の呼吸制御を定位照射に併用することも考えたが,治療時モニタが無い状態でマージンを小さくする試みは当面の方針に反すると考え採用しなかった。したがって,透視でITVを確認でき,かつ自然呼吸下でのPTVサイズがtolerableと判断される患者に適応を制限して,体幹部定位照射を開始した。
X線シミュレータ像を基本画像と決めたときまず問題になったのは,どのような患者セットアップ法がのぞましいか,透視画像をいかに治療計画に反映するか,というふたつである。部屋を変え,何度も患者セットアップを繰り返すには,再現性の高い患者固定具が不可欠である。当初は,頭頸部SRTの発想から,患者の可動性をできる限り奪うものが望ましいと考え,VAC-LOCで全身を埋め込んでしまうようなシェルを作成した。ここでの問題は,VAC-LOCと皮膚との摩擦が大きく,患者をシェルにセットするとき皮膚が強く引き攣れてしまうことである。皮膚マークにかわるセットアップの基準も検討したが,全てを置き換えることは困難で,それならば逆に皮膚マークのみを基準としその妨害因子を除去する方針とした。皮膚マークを最も干渉していたのは,VAC-LOCによる引き攣れと,挙上している上肢の位置再現性であった。そこで,シェルの形状を乗り降りが楽で皮膚を引っ張らないような薄型のものに変更し,ただ上肢だけは自作のグリップを握ってもらいながら入念に固定することとした(Fig. 2)。
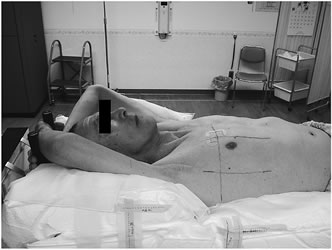
Fig. 2
|
X線シミュレータの透視画像を,CTシミュレータに基づく治療計画にいかに反映するかが,もうひとつの課題であった。機種選定時のプランとしては,X線シミューレーション,治療計画CT,放射線治療のすべてを同じ呼吸同期下に行うことで統一を図るという計画もあったが,Smart Gantry System搭載のCTが呼吸同期撮影に対応していないと判明し,問題外となった。実際には,まずX線シミュレータで観察後,1) ITVをradiopaque catheter等で皮膚にマーキングした上でCTを撮影する方法,2) 3秒スキャンCT(マシンが4秒スキャン不可)を行う方法,および3) 呼吸移動が十分小さいと判定されれば自然呼吸下の通常CT撮影,を用い治療計画データ収集をしている。従来は,治療計画後にそのままリニアック寝台上でマーキング,放射線治療を行っていたが,これでは実際のPTVの妥当性が透視画像で検証されていないのではと問題になった。そこで現在では,XiOで作成した治療計画をX線シミュレータ上でセットアップし,実際の治療門を透視で確認するというpost-RTP verificationのステップを加えることとした。ROIがマーキングされているDRR画像を参考にしながら,X線透視下に標的体積と照射野の関係を確認し,必要であれば微調整を加えて患者皮膚,Shellにマーキングを行っている。この時点で標的の動きをしっかり観察し,患者セットアップの基準となる静止画像を複数の呼吸相で記録しておくことで,治療時のリニアック グラフィとの照合がより確実になったと感じている。ただでさえ時間のかかる定位照射の準備に,新たにワン ステップを追加することになるため,当初は若干の反対があった。
|
症例
|
A
|
B
|
C
|
|
age/sex
Stage
組織型
部位
ECOG-PS
照射理由
|
82/male
cT1N0M0
SqCC
Lt. S4
0
2nd primary
Pulm Tbc |
76/male
cT1N0M0
SqCC
Rt. S6
0
CPEU
|
77/male
cT1N1M0
SqCC
Lt. S1+2/3
0
PAO critical
|
|
分割法
PTV
D95
V20
平肺線量
Follow-up
合併症肺炎
|
7.5Gy×8fx
59ml
53.8Gy
7%
9.7Gy
6 mo
grade 2 |
7.5Gy×8fx
29ml
55.3Gy
3%
6.3Gy
3 mo
− |
7.5Gy×fx
36ml
53.4Gy
4%
8.8Gy
On-going
− |
|
しかし実際に行ってみると,治療の基準となる画像が明確になり,標的が照射野の中をどのように動くかも確認済みであるので,照合のストレスが軽減され,全体としての治療時間も短縮することができている。
まだ3患者しか治療しておらず,経過観察も不十分であるため,意味のある治療成績は提示できない。1例に一過性のgrade 2肺臓炎がみられており,今後も全例を対象に定期的なfollow-upを続けていく予定である(Table)。
現在までの当科の照射方針は,6 MV以下のX線を用い,7門以上の固定多門照射,線量計算はsuperposition法で行い,治療スケジュールは12 Gy×4回照射もしくは7.5 Gy×8回照射(12 Gy/fxがriskyと判断された場合のみ)である(Fig. 3)。治療のoutcomeと各種照射パラメータとの相関を追跡していくことで,本治療の妥当性を検討するとともに,可能であれば現在厳しく制限している適応の再評価を行っていきたい。
以上,当センターにおける体幹部定位放射線治療の導入時経験を示した。治療成績を考えたとき,通常分割照射と比べた定位放射線治療の優位性は明らかと思われ,今後も積極的に実施していきたいと考えている。現在は,治療精度と安全性とのバランスを,適応症例を制限することで保証している段階である。症例を蓄積していくとともに,施設の拡充を図って,対象症例の適応拡大が今後の課題と考えている。
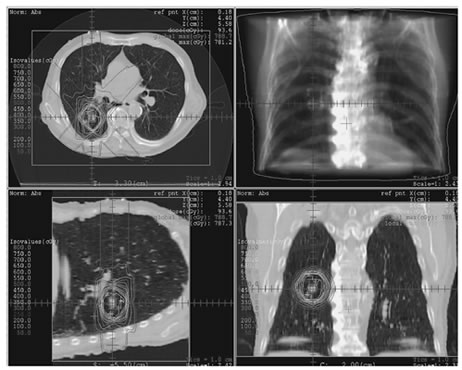
Fig. 3 |


